면역 관문 억제제에 의한 종양 표적 암 치료제 개발
의과대학 이창환 · 진준오 교수 연구팀
 왼쪽부터 이창환 교수, 진준오 교수, 박사과정 박해빈 씨
왼쪽부터 이창환 교수, 진준오 교수, 박사과정 박해빈 씨
[연구필요성]
광열 치료 기법은 새로운 종양 치료 기술로 종양을 열로 태워 제거하는 방법으로 각광 받고 있습니다. 하지만 종양을 표적하는 기술의 부족으로 높은 농도의 약물이 필요하며 부작용 또한 유발할 수 있는 문제가 있습니다. 또한, 종양은 수술적 치료가 가능하여 원발암의 치료 보다는 재발/전이암의 차단할 수 있는 치료제의 개발이 필요한 실정입니다. 따라서, 종양 표적성을 높이고 원발암을 치료할 수 있으며 전이 그리고 재발암을 막을 수 있는 새로운 치료제의 개발이 필요합니다.
[연구성과/기대효과]
울산대학교 진준오 교수 연구팀은 면역관문억제제를 이용한 종양 표적 지질 나노 구조체를 개발해 ACS Nano 저널에 발표하였습니다. 본 연구에서 해당 지질 구조체 (piLNP)는 암을 표적하여 광열치료 효과를 유도하는 것으로 원발암을 치료하였고 면역 관문 억제제의 면역 활성을 이용하여 전이암을 차단하는 효과를 나타내었습니다. 더 나아가 해당 지질 나노 구조체는 다양한 약물을 담지할 수 있어 화학 항암제부터 바이오 의약품까지 적용 가능할 것으로 기대됩니다.
[본문] - 연구 내용 요약
울산대학교 진준오 교수와 박해빈씨 (박사과정) 는 약물 담지에 사용할 수 있는 지질 구조체를 합성하였고 이 표면에 면역관문억제제의 항원 결합부위를 부착시키는 것으로 종양 표적성이 우수한 신규 약물 전달체를 개발하여 ACS Nano 저널에 발표하였습니다. 해당 논문에서는 지질 구조체를 합성할 때 광열제인 인도시아닌 그린 (ICG)를 담지하였고 표면에는 항 PD-L1 항체의 항원 결합 절편를 부착시켜 이를 piLNP라고 명명하였습니다.
해당 piLNP를 종양이 이식된 쥐 체내에 주입 하였을 때 PD-L1을 과발현하고 있는 종양을 표적하여 축척되는 것으로 나타났습니다. 이에 따라 내부에 담지 된 근적외선 레이져를 조사하였을 때 ICG가 반응하여 열이 발생하였고 종양이 효과적으로 제거 되었습니다.
이 과정에서 암 파편 (암항원)이 생산되었고 표적에 사용하던 항-PD-L1 절편이 면역 활성까지 유도하여 기억 세포를 활성 함으로서 재투여된 종양의 성장을 완벽하게 차단하였습니다.
[연구 결과]
Anti-PD-L1 Antibody Fragment Linked to Tumor-Targeting Lipid Nanoparticle Can Eliminate Cancer and Its Metastasis via Photoimmunotherapy
Hae-Bin Park, Eun-Koung An, So-Jung Kim, Dayoung Ryu, Wei Zhang, Chan-Gi Pack, Hyuncheol Kim, Minseok Kwak, Wonpil Im, Ja-Hyoung Ryu, Peter C. W. Lee, and Jun-O Jin
(ACS nano, 2024, 18, 33366−33380) (November 27, 2024) (https://doi.org/10.1021/acsnano.4c08448)
[용어 설명]
1. 면역관문억제제
면역관문억제제는 암세포가 면역체계를 회피하는 메커니즘을 차단하여 암에 대한 면역반응을 활성화 하고 면역세포가 암세포를 효과적으로 공격할 수 있도록 돕는 약물입니다.
2. 광열 치료제
특정 파장의 빛을 흡수하여 열을 발생시키는 물질로, 최근 암세포를 선택적으로 파괴하는 데 주로 사용되고 있음. 광열 치료제를 처리한 암 조직에서 국소적으로 열을 발생시켜 암세포를 죽이는 방식으로 작동합니다.
3. 기억 세포
면역체계에서 외부침입 항원, 체내 항원을 기억하며 재 노출시에 빠르고 강한 면역 반응을 유도하는 세포이다. 주로 T 세포, B 세포로 구성되며 초기 기억 이후 동일한 항원이 다시 나타날 경우 이에 대해 신속하게 방어합니다.
[그림설명]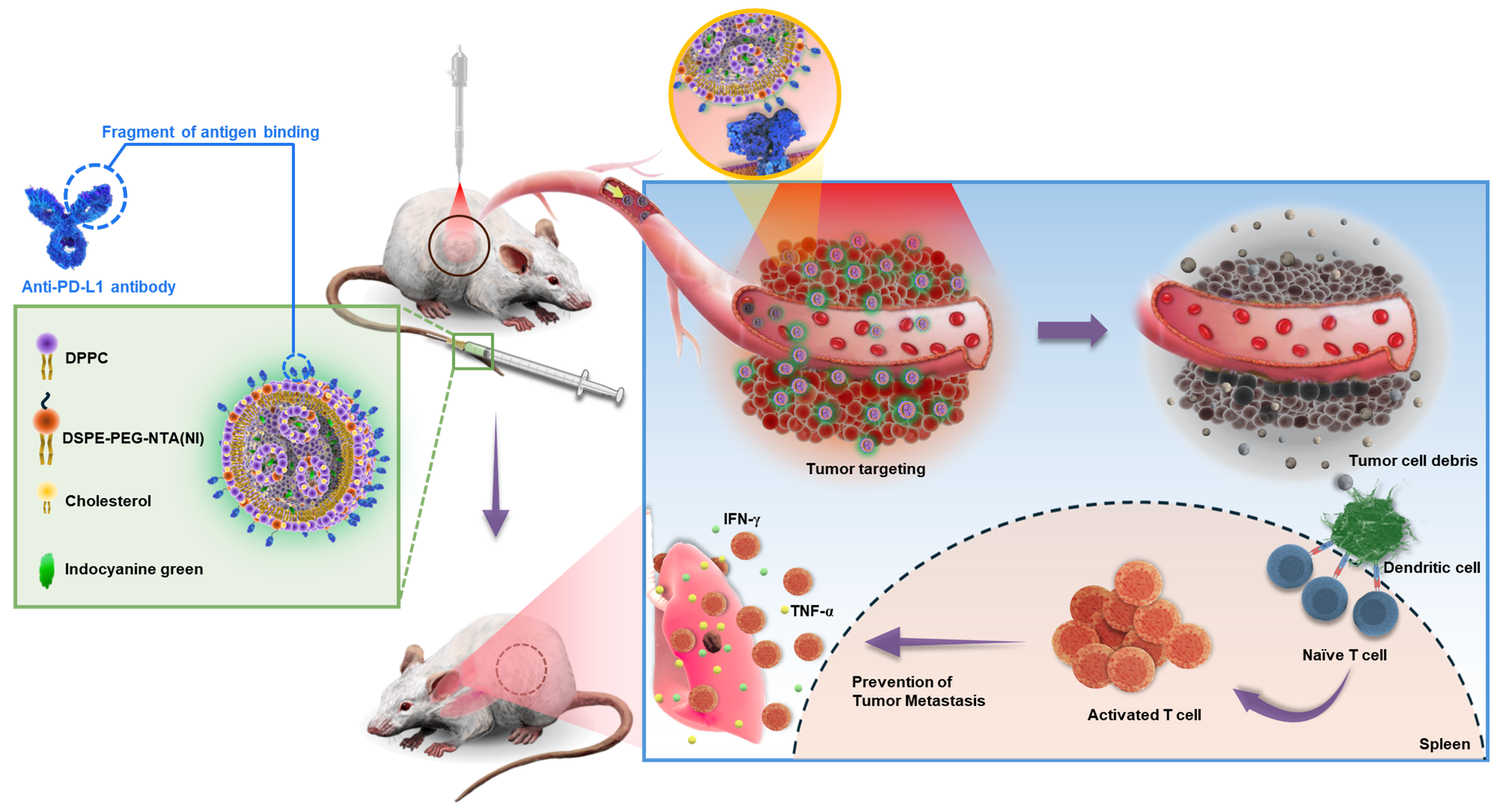 1. 항-PD-L1 항체 절편을 리피드 나도 구조체에 부착 후 마우스 체내 정맥 주사 하였다. 종양에 리피드 나노 구조체가 축적도니 것을 확인 후 NIR 레이저를 조사함.
1. 항-PD-L1 항체 절편을 리피드 나도 구조체에 부착 후 마우스 체내 정맥 주사 하였다. 종양에 리피드 나노 구조체가 축적도니 것을 확인 후 NIR 레이저를 조사함.
2. 항-PD-L1 항체 절편에 의해 암이 가진 면역 회피 작용이 차단되어 면역 활성 조건이 충족 되었고, 레이저에 의해 탄 암에서 항원이 나옴과 동시에 면역이 활성되면 암에 대한 정보를 면역세포들이 획득함으로써 암 전이 및 재발이 차단됨.
· 연구 시작 계기
광열치료는 종양의 완전 관해를 유도할 있는 매우 우수한 치료 방법임에도 불구하고 종양에 광열제를 효율적으로 전달하지 못해 그 효과가 미비한 경우가 많았습니다. 또한, 광열 치료 후에도 면역 활성이 충분하지 못하여 전이 및 재발암을 차단하지 못한다는 점에서 보다 종양 타겟과 함께 면역 활성을 유도할 수 있는 새로운 전달체를 개발하고자 본 연구를 시작하게 되었습니다.
· 연구과정 중 어려웠던 점
연구의 시작 단계에서 인도사이아닌 그린을 담지하고 항-PD-L1의 양을 충분하게 부착하기 위한 리피드 조성을 확립하는데 오랜 기간이 소요되었습니다.
· 타 연구와의 차별점
- 항 PD-L1 항체의 기능을 하는 부위인 절편 부위가 나노 구조체의 바깥 방향으로 노출될 수 있도록 하여 항 PD-L1 항체의 이용 효율을 높입니다.
광열치료제는 종양에 직접 투여하는 경우가 많으나 본 연구에서는 혈관 투여 후 종양에 축척되는 효과를 나타낼 수 있어 충분한 효율의 광열치료가 가능함과 함께 면역 활성까지 유도하는 일석이조의 효과를 나타냅니다.
